【寰宇新聞網/綜合報導】
日前傳出艾斯博有限公司委託仕成精密科技股份有限公司,在尚未取得GMP認證前,就擅自製造並供應7萬多支鈦合金骨釘骨板給全國醫療單位始用,食品藥物管理署在接獲通知後,已於9月10日要求艾斯博立即啟動產品回收。
根據食藥署表示,已接獲艾斯博公司繳交回收報告,共計回收75,299支骨釘、骨板,並由高雄市政府衛生局協助清點,仍有部分數量尚待釐清。
為確認回收作業確實完成,食藥署已於10月8日責成各地方衛生局至轄內醫療院所確認庫存狀況,案內產品於各醫療院所均已無庫存。
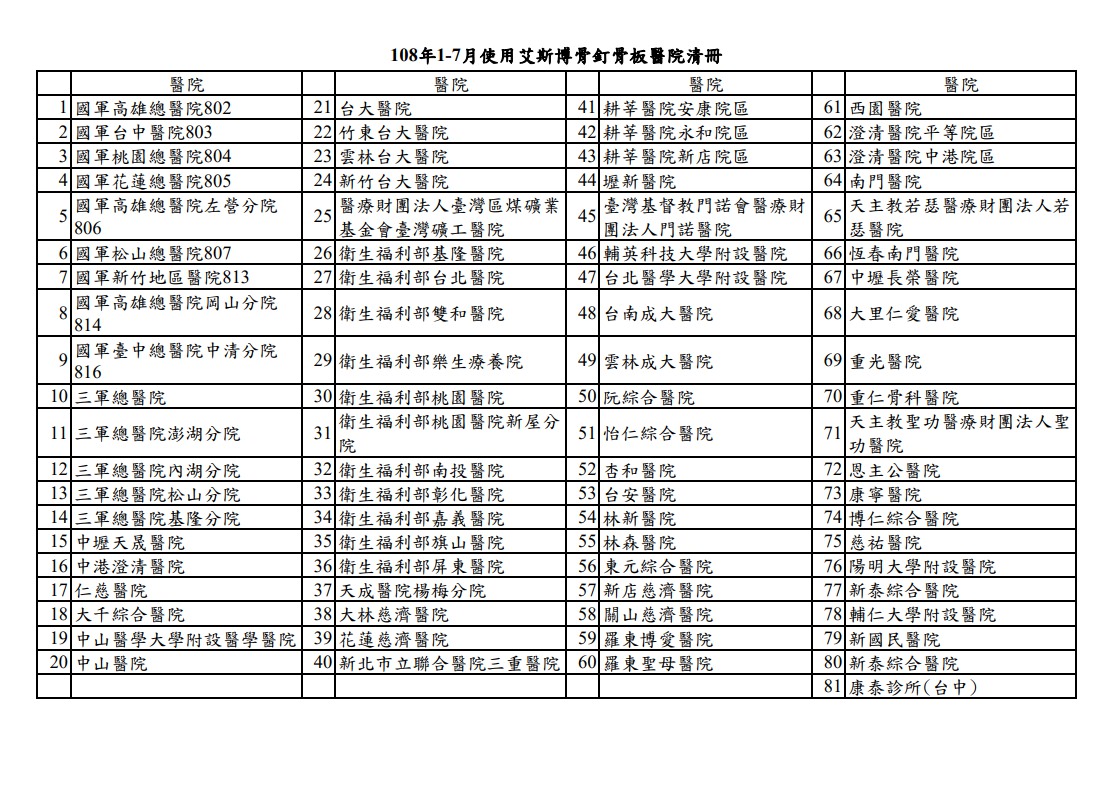
食藥署說,因無法釐清所使用產品是否屬合格製造廠製造,依食藥署現有掌握資料顯示,108年1月至7月間使用「喜維克骨釘骨板系統」(衛部醫器製字第004673號)」許可證產品之醫療院所共81家。食藥署將持續釐清產品回收狀況,倘回收作業未確實執行,涉違反藥事法第80條,將可對艾斯博有限公司處新台幣20萬到500萬元罰鍰。
食藥署提醒醫療院所持續關注使用該許可證產品之病人,若有疑似不良反應發生,請填具公告之醫療器材不良事件通報表,以傳真、郵寄或電子郵件( [email protected])通報的方式通報至全國藥物不良反應通報中心(地址:10092台北市中正區愛國東路22號10樓,電話:02-2396-0100,並請有疑慮民眾可至原就診醫院詢問專業醫療人員。
(圖片來源 : 食藥署網站)